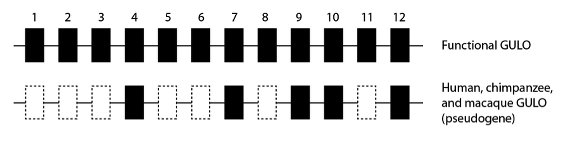Photo credit: Dallas Krentzel (Creative Commons Attribution 2.0 Generic)
Dans le dernier billet de cette série, nous avons examiné la diversification rapide de mammifères placentaux qui a suivi l’extinction des dinosaures non-aviens (causée par l’impact d’un astéroïde qui a marqué le passage du Crétacé au Paléogène il y a 66 millions d’années). Peu après cet événement (à l’échelle des temps géologiques), les primates apparaissent dans les données fossiles. Etant donné que notre propre espèce appartient aux primates (ce qui a d’abord été reconnu par Carl von Linné dans les années 1700), l’origine de ce groupe a considérablement intéressé les paléontologues.
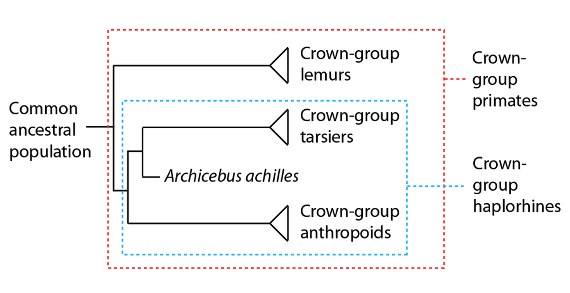
Pour le moment, le plus ancien primate que l’on connaisse est une toute petite créature qui vient du Paléogène médian de la Chine actuelle. Ce petit primate, Archicebus achilles, est un groupe couronne haplorrhinien qui a vécu il y a environ 55 millions d’années. Les Haplorrhiniens sont un groupe monophylétique où l’on trouve les tarsiers d’aujourd’hui ainsi que les espèces anthropoïdes : les singes du nouveau monde, ceux de l’ancien monde, et les grands singes, parmi lesquels se trouvent les humains. Les tarsiers et les anthropoïdes sont plus proches l’un de l’autre que des lémuroidea, un autre groupe de primates qui a des espèces encore en vie aujourd’hui :
Relations phylogénétiques au sein des groupes couronne des primates, qui montrent que l’Archicebus achilles a une position de groupe souche vis-à-vis du tarsier, proche de la base de l’arbre généalogique des primates.
Au-delà de son âge et de son statut actuel de plus ancien primate connu, Archicebus achilles est aussi remarquable en ce qu’il apparaît très proche de la dernière population ancestrale commune des lignages du groupe couronne des tarsiers et de celui des anthropoïdes, bien qu’il semble plus proche du lignage tarsier que du lignage anthropoïde (c’est-à-dire que même si Archicebus est proche du dernier ancêtre commun des tarsiers et des anthropoïdes, on le comprend mieux comme groupe souche des tarsiers). Les caractères d’Archicebus ainsi que sa localisation, proche de la base du lignage primate, suggèrent que la dernière population ancestrale commune était de façon similaire d’une petite stature, arboricole (qui vit sur les arbres), et se nourrissait d’insectes. La localisation d’Archicebus soutient aussi l’hypothèse selon laquelle les primates auraient d’abord évolué en Asie, et auraient migré plus tard en Afrique (où, comme nous le verrons dans un prochain billet, le lignage qui a conduit aux humains allait évoluera).
Au revoir GULO
C’est à la base de l’arbre généalogique des Haplorrhiniens qu’un événement a eu lieu et que nous avons déjà examiné comme étant une preuve forte en faveur de l’hypothèse de l’ancêtre commun de l’humain et du singe, événement que de nombreux chrétiens qui ont examiné les preuves pour l’évolution connaissent : un caractère partagé par les primates haplorrhiniens est leur curieuse incapacité à fabriquer leur propre vitamine C, ce qui les force à la chercher dans leur régime alimentaire. C’est inhabituel : la plupart des mammifères (y compris les primates non haplorrhiniens) sont capables de fabriquer leur vitamine C à partir d’un régime alimentaire basé sur du glucose. La raison génétique de cette déficience a été déterminée : chez les primates haplorrhiniens, l’enzyme qui permet cette dernière étape dans la biosynthèse de la vitamine C (nommée L-gulonolactone oxidase, ou “GULO”) est absente. Malgré le manque de cette enzyme et de sa fonction, on trouve des restes mutés du gène qui code l’enzyme GULO chez ces primates. Puisque cette déficience affecte tous les primates haplorrhiniens, l’explication la plus simple est que la fonction de l’enzyme a été perdue avant la séparation du groupe couronne haplorrhinien :
Afin d’apprécier les détails moléculaires de la perte de GULO dans le lignage haplorrhinien, revoyons brièvement la structure et la fonction d’un gène, ce que j’ai déjà examiné en détail ailleurs :
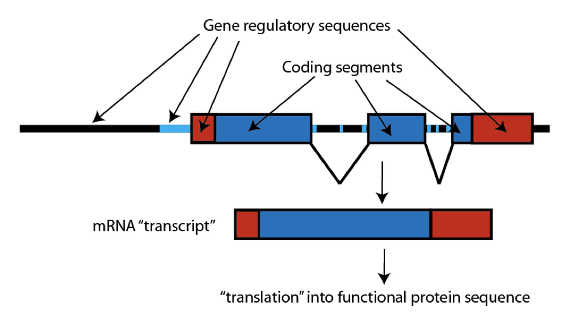
Les gènes ont une structure typique (que l’on simplifie ici). D’abord, il y a la séquence ADN qui spécifie la séquence qui produit les protéines (que l’on appelle la « séquence codante », en bleu). Cette séquence est habituellement cassée en segments dans les gènes des mammifères, et ces séquences sont recollées ensemble lorsque la séquence ADN du gène est transcrite en « copie de travail », nommée ARNm – une courte copie du code que la machinerie cellulaire peut utiliser pour construire la protéine spécifiée.
Le nom technique pour un segment de gène recollé et formé en ARNm est “exon” ; et les gènes fonctionnels GULO chez les mammifères ont douze exons. En comparant la séquence du gène GULO chez les grands singes (qui sont un groupe couronne haplorrhinien), nous voyons que de nombreux exons du gène GULO ont été entièrement supprimés, ce qui a rendu impossible la fonction. Chez les humains par exemple, seuls les exons 4, 7, 9, 10 et 12 demeurent ; et les chimpanzés et les macaques ont le même patron :
Diagramme schématique d’un gène GULO fonctionnel comparé à l’état observé chez plusieurs groupes couronne haplorrhiniens dont les données de la séquence du génome sont disponibles. Les mêmes sept exons sont supprimés dans le pseudogène GULO chez les humains, les chimpanzés et les macaques, détruisant la fonction de l’enzyme.
Il est peu probable que tous les événements de suppression de ces exons aient été les mutations à l’origine de la suppression de la fonction de ce gène dans le lignage haplorrhinien. Il est plus probable que ces suppressions aient eu lieu une fois que la fonction de GULO a été perdue, quand d’autres mutations de cette séquence (désormais non fonctionnelle) n’auraient pas de conséquences sur un gène déjà défectueux. Les suppressions partagées par les grands singes, cependant, ont eu lieu avant que les espèces se soient séparées, et ont été héritées par les espèces de ce groupe qui en ont résulté, de la manière que nous avons déjà examinée dans cette série, lorsque nous avons passé plusieurs billets à comparer les génomes à des manuscrits recopiés qui accumulent les erreurs au cours du temps.
Mutations partagées : un défi pérenne aux points de vue anti évolution
S’il est aisé de comprendre l’existence de gènes défectueux avec des mutations identiques dans des groupes d’espèces proches, cette question reste extrêmement difficile à expliquer pour les personnes anti évolution. En effet, le seul recours est d’essayer d’argumenter que les mutations identiques que nous observons chez de nombreuses espèces n’ont pas été héritées d’un ancêtre commun, et sont donc arrivées indépendamment dans chaque espèce. La probabilité que des mutations identiques aient lieu de nombreuses fois est bien entendu très petite, pour ne rien dire des patrons phylogénétiques précis que produisent de tels événements, prédits par d’autres lignes de preuves.
Donc, malgré la perte de GULO, et la nécessité conséquente d’une alimentation riche en vitamine C, le lignage anthropoïde a continué à s’étendre et à se diversifier. Dans le prochain billet de cette série, nous continuerons à examiner la diversification de ce groupe, et l’apparition de notre propre groupe en son sein : Homo.
Pour en savoir plus
- Lachappelle, M.Y. and Drouin, G. (2011). Inactivation dates of the human and guinea pig vitamin C genes. Genetica 139: 199-207. http://www.ncbi.nlm.nih.gov/pubmed/21140195
48 Articles pour la série :
- 01-L'évolution expliquée : Introduction
- 02-L'Evolution : Une théorie testée, pas une simple hypothèse !
- 03-Biogéographie
- 04-Une introduction à la variation, à la sélection naturelle et artificielle
- 05-Les chiens domestiques
- 06-Comment ça marche, la sélection naturelle ?
- 07-La sélection naturelle et le lignage humain.
- 08-Les bases de la variation héréditaire, première partie
- 09-Les bases de la variation héréditaire, deuxième partie.
- 10-De la variation à la spéciation (1)
- 11-De la variation à la spéciation (2)
- 12-De la variation à la spéciation 3
- 13-De la variation à la spéciation (4)
- 14-Les génomes sont comme des anciens textes (1)
- 15-Les génomes comparés aux textes anciens (2)
- 16-Les génomes comparés aux textes anciens (3): les origines de l'homme
- 17-Le génome comparé à un texte ancien (4)
- 18-Le génome comparé à un texte ancien (5): rattacher le tout ensemble.
- 19-Les arbres généalogiques des espèces, des gènes, et tri incomplet des lignées
- 20-Tri de lignage incomplet et taille d’une population ancestrale
- 21-Une introduction à l’homoplasie et à la convergence évolutive
- 22-Evolution convergente et homologie profonde.
- 23-Coévolution et la course à l’armement prédateur / proie
- 24-Le parasitisme, le mutualisme et la co-spéciation
- 25-Comprendre l’endosymbiose
- 26-La diversification cambrienne et la mise en place des plans d’organisation animaux. Première partie.
- 27-La diversification cambrienne et la mise en place des plans d’organisation animaux. 2e partie.
- 28-La mise en place des plans d’organisation des corps vertébrés, première partie.
- 29-La mise en place des plans d’organisation des corps vertébrés, deuxième partie.
- 30-La mise en place des plans d’organisation des vertébrés : Troisième partie.
- 31-La mise en place des plans d’organisation des vertébrés, quatrième partie.
- 32-Des reptiles aux mammifères.
- La révolution placentaire : deuxième partie. (Cet article)
- Du primate à l’humain, première partie.
- Du primate à l’humain, deuxième partie
- Du primate à l'humain (3)
- La paléontologie hominienne : une petite esquisse des preuves actuelles
- Devenir humain (1) : Eve mitochondriale et Adam Y-chromosomique
- Analogie entre évolution biologique et évolution du langage
- Devenir humain (3) : paléogénomiques et la toile emmêlée de la spéciation humaine
- 41-L’évolution, Partie 1: frontières scientifiques, abiogenèse et apologétique chrétienne
- 42-Aux frontières de l’évolution, Partie 2: l’abiogenèse et la question du naturalisme
- 43-Aux frontières de l’évolution, Partie 3 : l’hypothèse du monde à ARN
- 44-Aux frontières de l’évolution, partie 4 : Contingence versus convergence
- 45-Aux frontières de l’évolution, partie 5 : Contigence versus convergence dans l’expérience LTEE
- 46- L’évolution et le chrétien, première partie: Est-ce que l’évolution est un mécanisme sans but ?
- 47- L’évolution et le chrétien, deuxième partie: Une créature merveilleuse
- 48- L’évolution et le chrétien, partie 3 : Dire la vérité dans l’amour